LE QUOTIDIEN : La France accuse-t-elle un retard par rapport aux pays européens dans l'accès aux médicaments innovants ?
CLAUDE LE PEN : Officiellement, non. Les tutelles expliquent que la France reste un pays ouvert. Les médicaments innovants sont accessibles aux patients, même si nous sommes plus longs que les autres pays européens pour évaluer, tarifer, rembourser. Le délai entre l'autorisation de mise sur le marché (AMM) et la commercialisation peut durer des mois, voire même jusqu'à 200 à 250 jours alors que le délai légal européen est de 180 jours. Il existe même pour certains médicaments des années d’écart avec l'Allemagne et l'Angleterre ! Pire, faute d'accord sur le prix, des médicaments de la classe des glyphozines dans le traitement du diabète par exemple ne sont pas disponibles en France.
En 2016, un décret a revu les modalités de prise en charge des molécules innovantes, souvent onéreuses, inscrites dans la liste en sus (dispositif dérogatoire qui garantit un financement aux hôpitaux). Quel est l'impact de cette réforme ?
Dès qu’un médicament apporte des avancées thérapeutiques évaluées par la Haute autorité de santé (HAS), il doit être disponible. C’est un droit. À l’État ensuite de se débrouiller pour le financer, fixer le prix. Cela a été fait pour les médicaments contre l’hépatite C. À l’inverse, ce décret limite l'inscription des produits prescrits à l'hôpital sur la liste en sus. Cette inscription est désormais réservée aux médicaments reconnus comme apportant une amélioration du service médical rendu (ASMR) de I à III, excluant les médicaments à ASMR IV. Pour la première fois, on constate une rupture de l'équité républicaine dans l'accès aux médicaments innovants. Les patients ne sont pas prêts à accepter cette nouvelle doctrine.
L'enquête de « Décision santé » montre que certains hôpitaux n'hésitent pas à financer des médicaments à ASMR IV comme l'Avastin.
Ces médicaments présentent une certaine efficacité mais sont exclus de la liste en sus selon les nouvelles règles. Certains hôpitaux décident quand même de les financer sur leurs fonds propres, en prenant sur leur dotation annuelle, sur les enveloppes de recherche. Ces pratiques sont connues et sources d'inégalité entre les patients. L’État est conscient du problème et recherche une solution pour contrôler les dépenses sans pénaliser les patients. Sous leur pression, le décret « liste en sus » sera revu.
De nouvelles thérapies innovantes arrivent en cancérologie comme les CAR T-cells. Leur prix pourrait avoisiner 450 000 euros l'unité. Le mécanisme de fixation de prix à la française est-il pertinent pour ces innovations ?
Il faut prendre avec prudence les prix annoncés qui ne seront pas des prix réels, surtout aux États-Unis. En effet, le système de remises change la donne. En Europe, on est sur des prix beaucoup moins élevés. Aujourd’hui, les laboratoires qui ont des médicaments innovants ne négocient plus un prix avec le comité économique des produits de santé (CEPS). C'est un deal global. Les discussions portent sur les indications, une population cible, des protocoles, des règles de bon usage, des suivis des patients en vie réelle et des remises…
Faut-il réformer ce système ?
Ce système de fixation de prix trouve certaines limites. La vraie question n’est pas de fixer les prix des médicaments innovants chers dont on connaît les bénéfices thérapeutiques, mais de tarifer et de rembourser des innovations chères dont on ne connaît pas bien les bénéfices.
En principe, la valeur thérapeutique d'un médicament est déterminée par son développement clinique. Pour les médicaments traditionnels, ce développement dure en général dix ans. Pour les médicaments innovants, le délai est court, très rapide, avec un nombre de patients inclus dans une cohorte faible. Comment définir l'ASMR pour les produits dont le développement clinique est provisoire ? C'est un véritable défi pour tous les systèmes qui prennent en compte dans la fixation du prix la valeur thérapeutique. Dans la négociation des prix avec les industriels, il va donc falloir bricoler en jouant sur la population cible, les remises et la délivrance des molécules à certains centres de référence uniquement, tel l'Institut Montsouris (IMM).
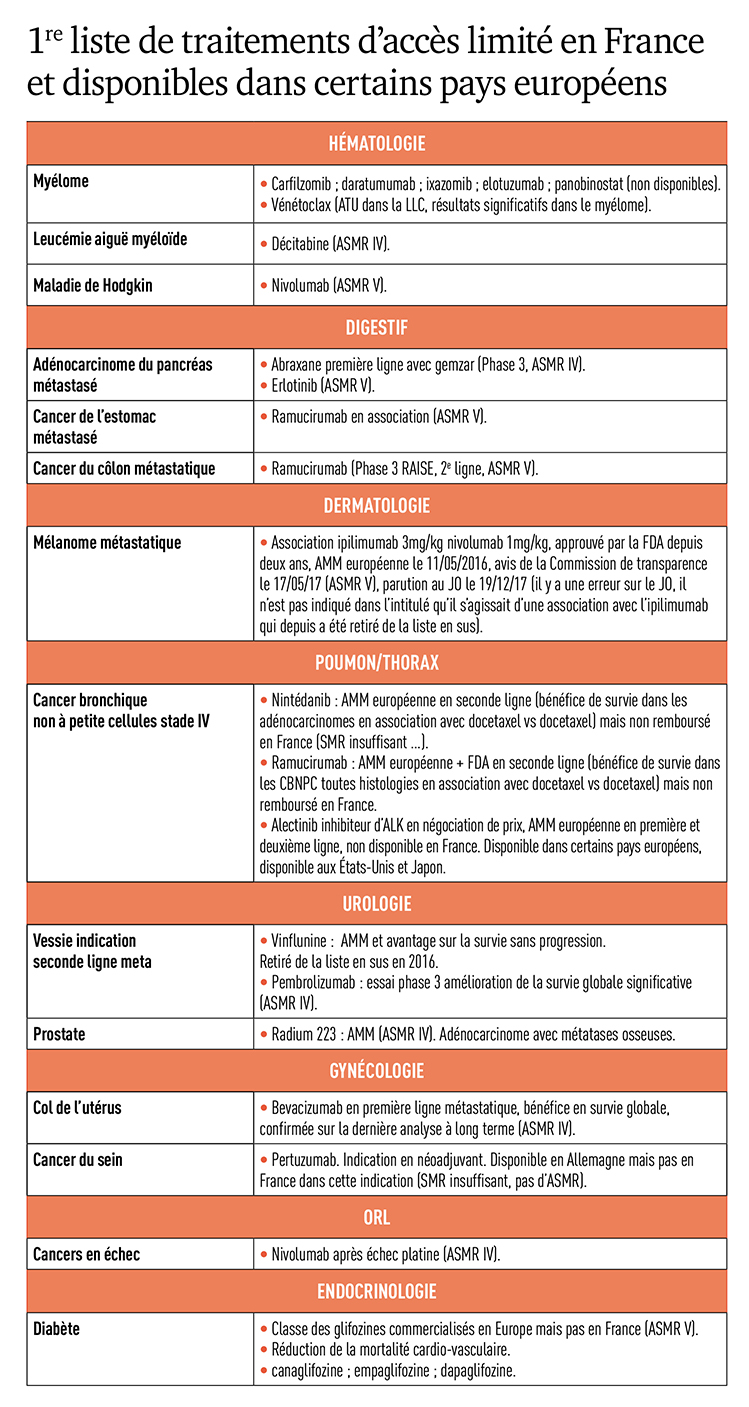
Source : « Décision Santé »


Violences sexistes et sexuelles : la Pr Agnès Buzyn se paye l’Ordre pour avoir « trop souvent protégé » les harceleurs
La santé publique doit être la deuxième priorité du Parlement européen, selon un sondage
Pas d’écrans avant 3 ans, pas de téléphone avant 11 ans… : la commission d’experts propose un guide fondé sur la science
Violences sexistes et sexuelles
Comment s’enracinent les schémas de domination à l’hôpital